
機能性表示食品とは
機能性表示食品とは、事業者が食品の安全性と機能性に関する科学的根拠を消費者庁に届け出ることで、機能性を表示することができる食品のことです。消費者が健康の維持や増進に役立つ食品を選びやすくすることを目的としています。
安全性・機能性の科学的根拠について国の審査は行われず、事業者の責任に基づいて適正な表示を行う、ということが大きな特徴です。特定保健用食品(トクホ)と異なり国が審査を行わないため、事業者は自らの責任で科学的根拠をもとにした適切な表示を行う必要があります。
機能性表示食品は、誇大広告や根拠の脆弱さについてたびたび問題となっていましたが、紅麹関連製品での問題をきっかけに「安全性」について大幅に規制が強化されることとなりました。

見直しの経緯
2024年(令和6年)春、紅麹関連製品による腎障害などの健康被害が相次いで報告され、サプリメントによる健康被害が社会問題となりました。制度の安全性や監視体制に対する不安が広がり、制度創設から10年目を迎える機能性表示食品制度の課題が、改めて浮き彫りとなりました。
届出された製品の科学的根拠には質のばらつきが見られ、表示の分かりにくさによって消費者が誤解する可能性も指摘されています。また、健康被害が発生した際の対応が十分ではないことも問題視されており、制度の抜本的な見直しが求められる状況となりました。
機能性表示食品の制度改正について
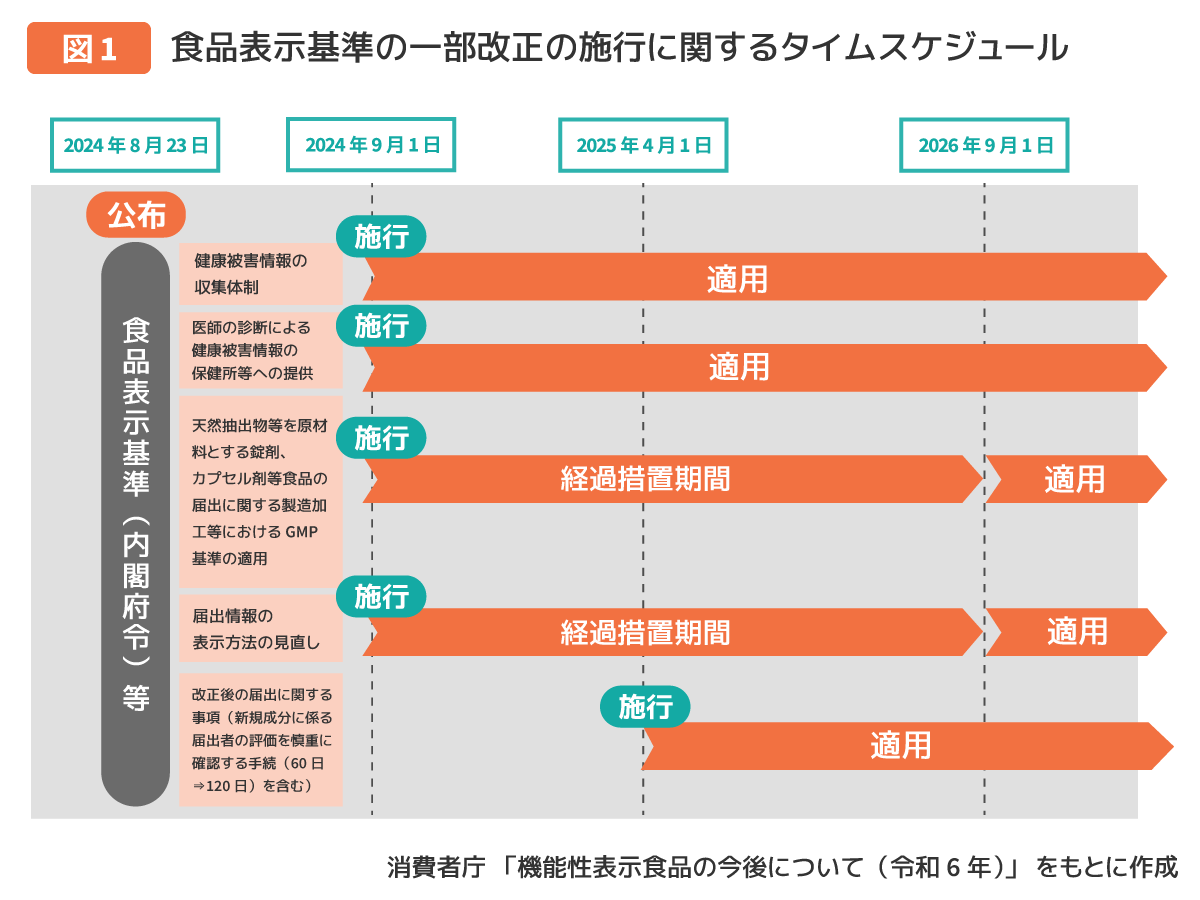
機能性表示食品に関する制度の見直しと施行期日については以下のようになっています。
①健康被害の情報提供の義務化に関しては即日実施ですが、②GMPの義務化、③表示方法の見直しなど、体制の整備が必要で早期実施が難しい項目については、2026年(令和8年)8月31日まで経過措置期間が設けられています。④届出確認期間の見直しについては、システマティックレビューの報告ガイドラインである「PRISMA2020」の導入にあわせ、2025年(令和7年)4月1日に施行されました。
見直しは単なる規制強化ではなく、「消費者の安全確保」「化学的根拠の明確化」「事業者の責任強化」を目的とした制度の信頼性向上を目指すものとなっています。
概要と事業者に求められる対応
以下に改正の概要と求められる対応についてまとめています。
健康被害の情報提供の義務化
紅麹製品の事案では、健康被害を把握していたものの消費者庁や自治体への報告に約2か月かかり、対応が遅れたことが問題視されています。これを受け、今後は健康被害情報の報告を義務化することとなり、食品表示法と食品衛生法における改正が2024年(令和6年)9月1日に施行、即日実施されました。
消費者から健康被害の連絡があった場合、医師の判断があるものなど一定の条件を満たす物は、保健所等の地方自治体および消費者庁に直接報告することを義務化する、と示されています。怠った場合は販売停止などの措置が取られる可能性があります。
食品表示法の対応
事業者は健康被害と疑われる情報を収集し、健康被害と疑われる情報(医師が診断したものに限る)を把握した場合、当該食品との因果関係が不明であっても速やかに消費者庁長官および都道府県知事等に情報提供することを、食品表示法に基づく内閣府令である食品表示基準における届出者の遵守事項とする。
食品衛生法の対応
食品衛生法に基づく食品衛生法施行規則においては、食品全般について、健康被害と疑われる情報(医師が診断したものに限る)を把握した事業者は都道府県知事等に情報提供するよう努めなければならないとされているが、機能性表示食品を製造・販売等する営業者(届出者)に対しては、食品衛生法施行規則において義務付けることとする。
GMPの要件化
製造工程管理による製品の品質確保を徹底する観点から、機能性表示を行うサプリメントについて、GMP(適正製造規範)に基づく製造管理が義務化されました。医薬品ではすでに義務化されているGMPの考え方が、今後は機能性表示のサプリメントにおいても適用されます。
こちらは、2024年(令和6年)9月1日施行、2026年(令和8年)9月1日実施となり、2年間の猶予期間が設けられています。
GMP(適正製造規範)とは
原料の入荷から最終製品の出荷に至るまでの全過程において、「適正な製造管理と品質管理」を求めるもの。
届出情報の表示方法の見直し
機能性表示食品の容器包装の表示情報についても見直しがされています。商品情報を消費者へ正しく伝えるために「機能性表示食品であること」が確認しやすい表記であることが重視され、食品自体に効果があると誤解されるような表記はできなくなります。
包材の切替等の事業者の実行可能性を考慮し、こちらも2年間の猶予期間が設けられており、2024年(令和6年)9月1日施行、2026年(令和8年)9月1日実施です。
ポイント
食品自体に効果があると誤解されるような表記は出来なくなります。
<例>
×コレステロールを下げる
〇この製品に含まれる●●には▲▼の機能があることが報告されています。
届出確認期間の見直し
機能性表示食品の届出確認期間についても見直され、2025年(令和7年)4月1日施行、即日実施されました。
新規の機能性関与成分については、届出資料をより慎重に確認するために、通常の60日間から120日間の期間が設けられることとなりました。
新規成分に係る届出資料を慎重に確認する手続きとして、表示内容の確認に時間を要すると消費者庁長官が認める場合に、特例として期間の延長と専門家からの意見聴取が行われます。

【まとめ】機能性表示食品制度の改正、対応時期を確認
機能性表示食品は届出のハードルやGMPの規制などが強化されます。健康被害情報の義務化、GMPの要件化、新規成分の通知期間の長期化、表示方法の改正が大きなポイントとなります。
今回の機能性表示食品制度の改正は、制度の信頼性を高めると同時に、事業者にとっては届出や表示の対応がより複雑になる転換点です。特に中小企業にとっては、限られたリソースの中で制度対応を進める必要があり、事前の準備と情報収集がこれまで以上に重要となります。制度のポイントを押さえ、計画的に対応すれば、消費者からの信頼を得るチャンスにもなります。今後も継続的に動向をチェックし、適切な対応を行っていきましょう。
食品ITNAVIでは食品業事業者さまに向けて最新情報の提供に努めています。続報についても随時お伝えしてまいりますので、ぜひメルマガやSNSでチェックしてください!
よくある質問
- Q.機能性表示食品制度とは何ですか?
- A.機能性表示食品制度は、化学的根拠に基づいて特定の機能性を表示することができる食品の制度です。消費者庁に届出を行うことで、機能性表示が可能となります。
- Q.GMPとは何ですか?
- A.GMPとは、**Good Manufacturing Practice(適正製造規範)**の略で、医薬品や食品、化粧品などの製造において「安全で高品質な製品を一貫して製造するための基準や管理方法」を定めたものです。日本では、厚生労働省がGMPに関する基準を定めており、製造業者はこれに従う必要があります。
- Q.届出確認期間の見直しとは何ですか?
- A.届出確認期間の見直しは、機能性表示食品の届出に関する手続きや確認期間を見直す改正です。新規成分に係る届出資料の確認手続きが強化され、提出期限が販売日の120営業日前とされました。
【参考】
・消費者庁(平成27年)「機能性表示食品制度がはじまります」
・消費者庁(令和6年)「機能性表示食品の今後について」
・消費者庁(令和6年)「機能性表示食品等に係る健康被害の情報提供の義務化について」
・消費者庁「機能性表示食品について」








